Raul Bonne Hernández, professor de Química Ambiental e Toxicologia no Instituto de Ciências Ambientais, Químicas e Farmacêuticas (ICAQF/Unifesp) – Campus Diadema, e outros pesquisadores da Universidade Federal de Santa Catarina (UFSC), do Instituto de Pesquisas Biomédicas de Barcelona (CSIC) da Universidade Autônoma de Barcelona e do Centro de Saúde Ambiental da rede Helmholtz (Alemanha) foram premiados em dois grandes eventos promovidos pela Sociedade Brasileira de Toxicologia (SBTox) por pesquisa inédita que identifica rotas metabólicas do manganês (Mn). O estudo analisou como o metal induz à neurotoxicidade em culturas primárias de células granulares de cerebelo (CGCs, um modelo in vitro).
Considerado um sal mineral de extrema importância ao metabolismo humano, o manganês pode ser perigoso: a ingestão crônica de quantidade diária superior a 3mg, porção adquirida pela ingestão de alimentos como oleoginosas (vegetais que possuem óleos e gorduras – amendoim, castanhas, amêndoas, milho, girassol, etc), comumente leva a um quadro de intoxicação conhecido por manganismo. Sabe-se hoje que o distúrbio provoca permanentemente tremores, dificuldades de coordenação motora e problemas de memória.
Apesar de sua toxicidade ser conhecida há mais de 100 anos, ainda é nebuloso à ciência o modo como esse elemento provoca alterações nas diferentes vias metabólicas - conjunto de reações químicas para manutenção do equilíbrio dinâmico necessário à sobrevivência dos organismos. “Hoje, o que temos são diversas hipóteses que sugerem uma associação entre a exposição ao manganês e o desenvolvimento futuro de doenças relacionadas à neurotoxicidade, especialmente durante o período perinatal (compreendido entre a 28ª semana de gestação e o sétimo dia de vida do recém-nascido) e o infantil”, explica o professor da Unifesp.
De forma a preencher essa lacuna, os pesquisadores optaram por uma abordagem inovadora. Aliando a proteômica, estudo da expressão proteica em células e tecidos, e a metalômica, análise da influência dos metais em genes, proteínas, metabólitos e outras biomoléculas, eles avaliaram os efeitos tóxicos do cloreto de manganês (MnCl2) e dos fungicidas maneb (C4H6MnN2S4) e mancozeb (C8H12MnN4S8Zn) em culturas primárias de CGCs.
Metodologia
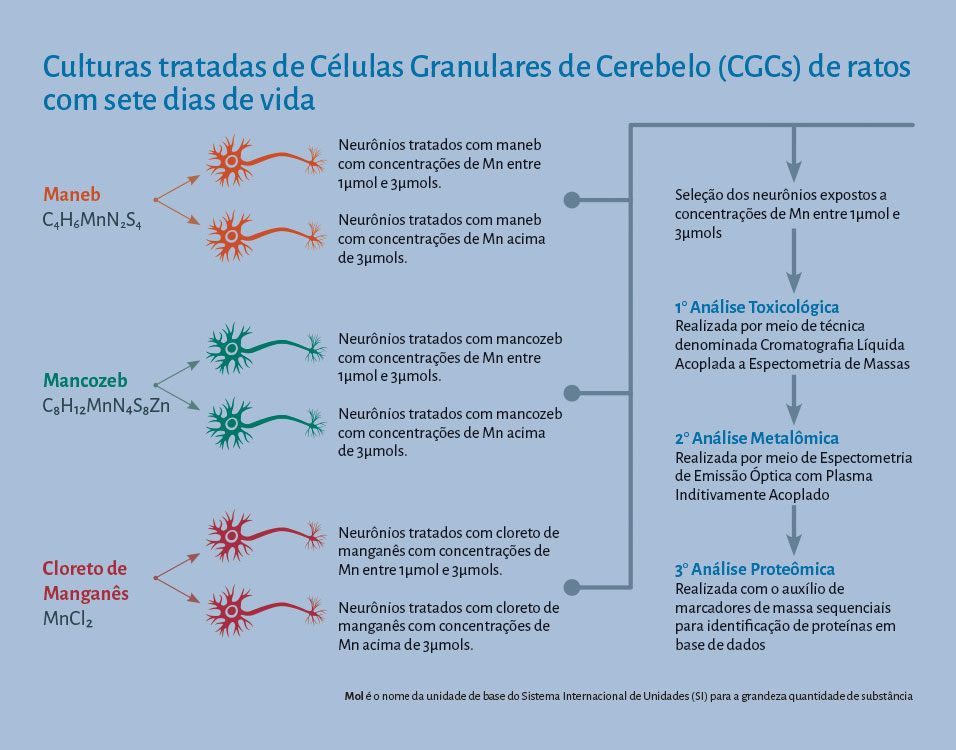
As células utilizadas foram extraídas de cerebelos de ratos com sete dias de vida, época em que ocorre a neurogênese (sequência de eventos que leva à formação do sistema nervoso) nesses animais, o que garantiu a aquisição de neurônios em estágio indiferenciado. Uma população dessas CGCs foi exposta a crescentes quantidades dos compostos à base de manganês durante diferentes períodos de tempo e em diferentes estágios de desenvolvimento (gráfico na página seguinte). Entretanto, Bonne explica que apenas as células expostas a concentrações entre 1 e 3 mols de manganês (quantidades não tóxicas), foram submetidas à análise toxicológica e, posteriormente, aos estudos de metalômica e proteômica.
Conclusões
Os estudos toxicológicos revelaram que a exposição crônica de CGCs ao maneb, ao mancozeb e ao cloreto de manganês (MnCl2), em estágios iniciais de diferenciação celular, é mais importante do que a exposição aguda, pois a bioacumulação ocorreu apenas em amostras tratadas com pequenas quantidades dos compostos por um longo período de tempo. Mas os efeitos negativos estendem-se além dessas conclusões, segundo Bonne.

O professor Raul Bonne Hernandez, do Departamento de Ciências Exatas e da Terra do ICAQF/Unifesp

As análises laboratoriais de células granulares de cerebelo aliaram a metalômica e a proteômica
“No caso do MnCl2, o manganês depositado gradativamente nas células neuronais alterou definitivamente a homeostase de outros metais necessários ao seu funcionamento. Isso porque os pesticidas em questão levaram a uma diminuição dos níveis de ferro (Fe), potássio (K) e cálcio (Ca). Sendo metais muito importantes ao funcionamento celular, é evidente que a neurotoxicidade por manganês induz a diversos distúrbios, culminando inclusive na apoptose (morte celular programada)”, revela ele, baseando-se na metalômica.
Já a análise proteômica trouxe dados mais complexos. Considerando que o metabolismo de cada célula envolve a ação ou mesmo a modificação de proteínas, a exemplo das enzimas (catalisadoras de reações químicas) e das proteínas (agentes passivos das enzimas), o estudo mostra que algumas delas foram efetivamente influenciadas pela presença de Mn e, consequentemente, alteraram o funcionamento celular.
“O cloreto de manganês agiu diretamente em classes importantes de enzimas, a saber dihidropirimidinase e piruvato quinase, responsáveis, respectivamente, pelo equilíbrio da oxidação nas células e pela produção de adenosina trifosfato (ATP) – nucleotídeo que armazena energia proveniente da respiração celular”, especifica o professor.
O maneb, por sua vez, alterou o funcionamento das proteínas EIF5A e CRMP2, associadas com a expressão gênica e o transporte de aminoácidos através da membrana celular, e induziu a uma regulação negativa da proteína transmembranar TMEM132A, expressa no retículo endoplasmático, aparelho de Golgi e membrana celular. Segundo Bonne, esta última merece atenção especial por regular o processo de apoptose. “Expressa durante o período embrionário e estágios pós-natal do desenvolvimento do cérebro do rato, a TMEM132A está envolvida com o transporte intracelular de cálcio”.
Outra descoberta viabilizada pela proteômica, reforçando os efeitos fatais do Mn às células, foi a superexpressão do EIF4B, envolvido na tradução de RNAm. Houve, nesse caso, uma expressão aumentada entre 25 e 50 vezes, o que, segundo estudos da equipe, leva ao efeito inverso, ou seja, provoca a inibição da síntese proteica. As consequências disso são diminuição da sobrevivência celular devido à ativação de sinais pró-apoptóticos.
“O manganês proveniente desses compostos culminou em problemas de metabolismo energético e alteração na homeostase de metais nessas células, fatores que desencadeiam deterioração e morte celular. Hoje, podemos dizer que as rotas metabólicas alteradas pelo Mn são de fato mais claras, o que traz novas perspectivas a pesquisadores do mundo todo”, avalia Bonne. Ele enfatiza, finalmente, que a equipe continua trabalhando no aprimoramento desses estudos. A perspectiva é identificar alterações metabólicas induzidas pelo manganês em demais espécies, incluindo o ser humano.
Muito além do manganismo
Segundo o professor do ICAQF da Unifesp, o manganês poderia estar envolvido em mais doenças neurodegenerativas, além do manganismo, como o Parkinson e o Alzheimer. “Sabe-se, hoje, que as alterações no metabolismo de proteínas e na expressão gênica do DNA, em células cerebrais e terminações nervosas, podem levar ao desenvolvimento desses distúrbios, e o Mn poderia estar provocando isso”, explica Bonne. A má notícia é que a acumulação do metal em indivíduos saudáveis estaria ocorrendo por sua alta incidência na água e no solo.
A poluição dos sistemas aquáticos por elementos-traço, que ocorrem naturalmente em níveis de parte por milhão (ou abaixo disso), vem sendo reconhecida como um problema que pode representar riscos à saúde humana e ao meio ambiente. A Organização Mundial da Saúde (OMS), de um lado, recomenda 400 microgramas por litro de água para consumo humano como limite toxicológico. Já para o Conselho Nacional do Meio Ambiente (Conama), o limite a ser seguido é de 100μg /L.
Em reservatórios do Estado de São Paulo, a concentração de manganês encontra-se dentro do limite nacional. “No entanto, os estudos têm apontado alterações neurocomportamentais mesmo em indivíduos expostos a essa quantidade”, explica Bonne. “Nas águas do volume morto do sistema Cantareira, mais próximas do solo, esses índices podem ser maiores, porém hoje não há um relatório conclusivo”.
O manganês proveniente do sulfato de manganês e do cloreto de manganês, presentes no solo, reage com a água formando um complexo (1Mn6H20), que penetra facilmente no organismo humano, pois os íons de manganês ficam relativamente livres entre as moléculas de água. “Dissolvido, o metal atravessa a massa cefálica, acumulando-se gradativamente no cérebro, levando à neurotoxicidade”, explica.
Para ele, as maiores vítimas da intoxicação por elementos-traço são as comunidades sem acesso a sistema de tratamento e distribuição de água adequados. “As filtragens convencionais são eficientes para a remoção de grandes quantidades de manganês. Além disso, entre esse processo e o trajeto até nossas casas, o metal é muito suscetível à oxidação pelo solo, o que contribui para diminuir sua concentração na água”, complementa Bonne. No entanto, permanece o desafio de aperfeiçoar esses sistemas para que removam quantidades que, embora inferiores ao limite de 100 μg /L, ainda oferecem riscos à saúde humana. “Hoje estamos afunilando os estudos no desenvolvimento de um sistema de remoção de traços de manganês”.





